Sublimação e Evaporação: Uma Visão Geral: De Um Exemplo De Sublimação E Um De Evapora Ao
De Um Exemplo De Sublimação E Um De Evapora Ao – Sublimação e evaporação são dois processos físicos que envolvem a mudança de estado da matéria. Embora ambos levem a uma transformação de fase, eles diferem significativamente em seus mecanismos e condições necessárias. Este artigo irá explorar esses processos, fornecendo exemplos do cotidiano e comparando suas características.
Introdução à Sublimação e Evaporação
A sublimação é a transição direta de uma substância do estado sólido para o estado gasoso, sem passar pelo estado líquido intermediário. Já a evaporação é a transição de uma substância do estado líquido para o estado gasoso. A principal diferença reside na mudança de estado físico: sublimação (sólido para gasoso) versus evaporação (líquido para gasoso). A taxa de ambos os processos é altamente dependente da temperatura e pressão.
Em temperaturas mais altas e pressões mais baixas, tanto a sublimação quanto a evaporação ocorrem mais rapidamente. A sublimação, entretanto, tende a ser mais lenta que a evaporação sob condições normais, pois requer mais energia para quebrar as forças intermoleculares no estado sólido.
Exemplos de Sublimação, De Um Exemplo De Sublimação E Um De Evapora Ao

Existem diversos exemplos de sublimação na vida cotidiana. Aqui, analisaremos três exemplos concretos, destacando suas características e aplicações.
| Substância | Temperatura de Sublimação (aproximada) | Aplicação Prática | Observações Relevantes |
|---|---|---|---|
| Gelo Seco (CO2 sólido) | -78.5 °C | Refrigeração, efeitos especiais em teatro e cinema | Sublima rapidamente, formando névoa densa de dióxido de carbono. |
| Naftalina | Variável, dependendo da pressão | Repelente de insetos | Sublima lentamente, liberando vapores que repelem insetos. O processo é mais rápido em ambientes quentes. |
| Iodo | 113.7 °C (a 1 atm) | Reações químicas, desinfecção | Produz vapores violeta característicos durante a sublimação. |
A sublimação do gelo seco é particularmente interessante. O dióxido de carbono sólido, ao sublimar, transforma-se diretamente em gás carbônico, criando uma névoa densa e fria. Isso ocorre porque o gás carbônico resfria o ar ao redor, causando a condensação da umidade presente no ar, formando pequenas gotículas de água que compõem a névoa.
Exemplos de Evaporação
A evaporação é um fenômeno comum, observável em diversas situações do dia a dia. A seguir, apresentamos três exemplos práticos, detalhando o processo em cada caso.
- Secagem de roupa: A água líquida presente na roupa passa para o estado gasoso devido ao calor do sol ou de uma secadora, reduzindo a umidade do tecido.
- Formação de nuvens: A evaporação da água dos oceanos, rios e lagos gera vapor de água que, ao ascender e resfriar, condensa formando nuvens.
- Evaporação da água do mar: A água do mar evapora constantemente, impulsionada pela energia solar. A temperatura, a umidade e o vento influenciam diretamente a taxa de evaporação. Temperaturas mais altas, baixa umidade e ventos fortes aceleram o processo. A evaporação da água do mar é um processo fundamental no ciclo hidrológico, deixando os sais dissolvidos para trás e contribuindo para a formação de nuvens.
Sublimação x Evaporação: Um Estudo Comparativo
Tanto a sublimação quanto a evaporação requerem energia para ocorrer, mas a quantidade de energia necessária difere. A sublimação exige mais energia do que a evaporação, pois é preciso romper as ligações mais fortes presentes no estado sólido. Ambas as transições de fase estão relacionadas à pressão de vapor da substância. A sublimação ocorre quando a pressão de vapor do sólido excede a pressão atmosférica, enquanto a evaporação ocorre quando a pressão de vapor do líquido excede a pressão atmosférica.
As semelhanças incluem a mudança de estado físico para gasoso e a dependência da temperatura e pressão.
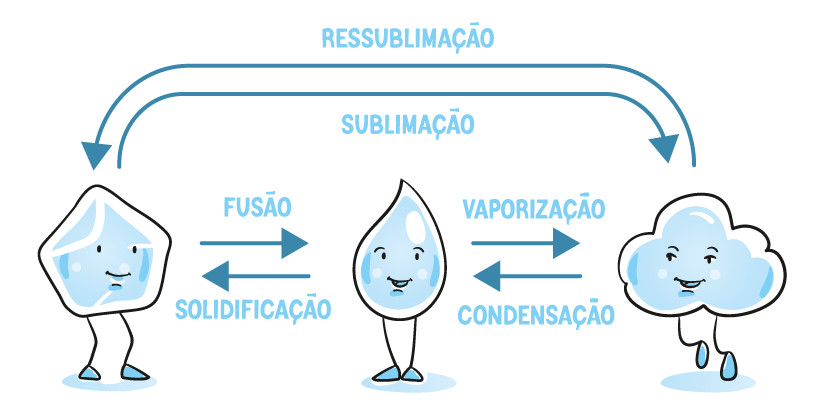
Um diagrama simples poderia representar isso: Imagine um diagrama de fases com os estados sólido, líquido e gasoso representados por regiões distintas. A sublimação seria representada por uma seta partindo da região sólida diretamente para a região gasosa. A evaporação seria representada por uma seta partindo da região líquida para a região gasosa. As setas indicariam a direção da mudança de fase, e rótulos poderiam indicar a temperatura e pressão necessárias para cada transição.
A energia envolvida em cada processo poderia ser representada pela inclinação ou comprimento das setas.
Aplicações Práticas da Sublimação e Evaporação
A sublimação encontra aplicações importantes em diversas indústrias. Na indústria têxtil, a sublimação é usada para imprimir imagens em tecidos sintéticos. Na produção de microchips, a sublimação de materiais específicos é empregada para deposição de filmes finos. A evaporação é crucial em processos como a produção de sal marinho (através da evaporação da água do mar), a secagem de produtos agrícolas e a concentração de soluções.
Em resumo, o entendimento profundo de ambos os processos é fundamental em várias áreas, desde a química e a física até a engenharia e as ciências ambientais.
Qual a principal diferença entre sublimação e evaporação?
A sublimação é a transição direta de sólido para gasoso, enquanto a evaporação é a transição de líquido para gasoso.
A sublimação ocorre apenas com determinadas substâncias?
Sim, a sublimação é mais comum em substâncias com alta pressão de vapor no estado sólido, como o gelo seco e a naftalina.
A evaporação é afetada pela pressão atmosférica?
Sim, a evaporação ocorre mais rapidamente em pressões atmosféricas mais baixas, pois a pressão parcial do vapor é menor.

